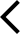加错试剂却迎来重大突破:创造电解水制氢催化剂新纪录
一款新型催化材料被浸在碱性水中,表面持续不断地产生气泡,在高安培电流密度下,它已经稳定运行超过19000小时。这意味着,经过两年以上的连续运行,这个小小方块毫无衰退的迹象。 这是阴离子交换膜电解水制氢(AEM-WE)的实验现场。之前,AEM-WE技术因氧气析出反应(OER)催化剂在高电流密度下难以持久而未能实现商业化。然而,西湖大学人工光合作用与太阳能燃料中心(CAP)在这一材料上获得重大突破。经过长期的探索和一次意外的实验,他们神奇地解决了这一难题,仿佛得到了天赐的助力。 最近,西湖大学孙立成教授团队在Nature Catalysis(《自然·催化》)上发表了他们的研究成果。他们开发了一种新的催化剂制备技术,该技术基于非均匀形核液相体系,即向溶液中人为引入不溶纳米颗粒,并在常温、常压条件下通过简单的浸泡法,一步合成非贵金属催化剂——CAPist-L1。 氢气无疑是清洁、高效、可持续的能源,其燃烧过程中只产生水,并且所释放的热量是天然气的2.56倍,更是普通汽油的2.95倍。 氢元素广泛存在于自然界中,通常以水的形式存在,而光合作用就具有将水分子"分解"的神奇能力。 孙立成教授的团队在过去二十多年里,一直致力于研究并模仿自然界的这种分解能力,他们在光合作用和清洁能源领域取得了一系列重大进展。例如,他们开发了Ru-bda这种新型催化剂,并揭示了光合作用中"椅子魔术"的关键环节。 电解水制氢实验室一角 学过初中化学都知道,通过电解水可以分离出氢气和氧气。但这个过程如果没有催化剂的辅助,将消耗大量的电能,从经济角度来看并不可行。 目前,低温电解水制绿色氢气技术主要分为:碱性电解槽电解水制氢(AWE)、质子交换膜电解水制氢(PEM-WE)、阴离子交换膜电解水制氢(AEM-WE)。 其中,AEM-WE融合了前两种技术的优势,被广泛看好。简单来说,AEM-WE系统通过阴离子交换膜将氧气和氢气的产生区域分隔开,在阳极催化剂的作用下产生氧气,而在阴极催化剂的作用下产生氢气。然而,阳极侧OER催化剂在高电流密度下难以保持高活性和稳定性。而根据化学反应的守恒定律,每两份氢气的形成必然伴随着一份氧气的生成。因此,阳极催化剂的催化效率成为了制约AEM-WE技术发展的关键因素。 电解水实验装置(CAP) 而一次"错误"却带来的神奇的突破。孙立成介绍,在一次实验中,团队成员在制备镍铁基的OER催化剂时,误将乙醇(酒精)用作溶剂,却意外地发现这种在泡沫镍上生长的催化剂展现出了卓越的OER性能。在电镜视角下,这种催化剂酷似层层花瓣叠加的花朵,因此被赋予了"绣球花"这一美丽的名字。 CAPist-L1催化剂的“绣球花”结构 基于“绣球花”良好的催化表现,研究团队研究团队立即从理论角度进行了探究,并逐步完善了制备方案,开发出了一种基于非均匀形核液相体系的催化剂制备技术。在催化机理的研究上,通过对CAPist-L1的组成、结构和形态进行详尽分析,研究团队发现了催化层与金属基底之间存在一层致密的过渡层。正是这层致密的过渡层有效地将催化层锚定在金属基底上,增强了催化剂的活性和耐久性。 CAPist-L1,材料呈现多孔的透气结构 值得期待的是,CAPist-L1因其制备工艺的简便性、成本的低廉性、高可重复性、易于规模化生产以及超高的OER活性和稳定性,展现出了巨大的工业化应用前景。 前衍可提供产品 7720-78-7 硫酸亚铁 64-17-5 乙醇 67-63-0 异丙醇
2024-09-19
美国最昂贵的10 种药物
世界上最昂贵的10种药物,生命无价,每一款药物的诞生,都是对生命价值的最好诠释。药物的诞生过程,从最初的构想到最终的上市,就像一场与时间竞赛的长跑。据统计,一款药物从研发到上市平均需要15年的时间。然而,部分药物的价格之高令人咋舌,单次治疗的费用甚至可达数百万美元。尽管一些制药企业已经自愿下调了部分药品的价格,但这个行业的新产品仍在不断刷新价格上限。在公众对药品成本问题日益关注的情况下,药品定价的改革之战仍在继续,旨在为患者争取更合理的药物成本。 1、Lenmeldy 公司: Orchard Therapeutics 疾病:异染性脑白质营养不良 (MLD) 每次治疗: 425 万美元 FDA 批准日期:2024 年 3 月 18 日 Lenmeldy (atidarsagene autotemcel) 是一种自体造血干细胞 (HSC) 基因疗法,用于治疗异染性脑白质营养不良 (MLD) 儿童。Lenmeldy 是 MLD 的第一种治疗方法,有可能通过单一治疗恢复酶功能以阻止或减缓这种致命疾病。Lenmeldy 将在美国一些州的合格治疗中心进行。 根据 Orchard Therapeutics 的数据,Lenmeldy 的批发收购成本 (WAC) 将为 425 万美元,使其成为目前美国最昂贵的药物。Orchard 的官员引用了治疗对患者及其家人的价值、可能的护理人员工资损失以及降低医疗保健利用率的可能性。 2、Hemgenix 公司:CSL Behring, uniQure 疾病:血友病 B 每次治疗:350 万美元 FDA 批准日期:2022 年 11 月 22 日 Hemgenix (etranacogene dezaparvovec-drlb) 被批准用于治疗血友病 B,这是一种罕见的终身出血性疾病。作为单次一次性静脉内 (IV) 输注,它的标价为 350 万美元。它允许 B 型血友病患者产生自己的 IX 因子(一种凝血因子),并且可以降低单剂量出血的风险。 B 型血友病是一种罕见的终生出血性疾病,由单基因缺陷引起,导致因子 IX 产生不足,因子 IX 是一种主要由肝脏产生的蛋白质,有助于形成血栓。患有这种疾病的人特别容易出现关节、肌肉和内脏器官出血,从而导致疼痛、肿胀和关节损伤。通常,B 型血友病患者必须遵守严格、昂贵、终身输注因子 IX 的计划。 Hemgenix 是一种基于腺相关病毒载体的基因疗法。它的工作原理是提供非感染性病毒载体 (AAV5) 将遗传 DNA 指令携带到肝脏,然后在那里产生因子 IX 蛋白。这些遗传指令保留在靶细胞中,但通常不会成为一个人自身 DNA 的一部分。 3、Elevidys 公司:Sarepta Therapeutics 疾病:杜氏肌营养不良症 (DMD) 每次治疗:320 万美元 FDA 批准日期:2023 年 6 月 22 日 Elevidys (delandistrogene moxeparvovec-rokl) 被批准用于治疗 4 至 5 岁患有杜氏肌营养不良症 (DMD) 且已确认 DMD 基因突变的儿童。它以一次性单剂量静脉内 (IV) 输注的形式给药,价格为 320 万美元。选择治疗的患者具有抗 AAVrh74 总结合抗体滴度 <1:400。Elevidys 不应用于 DMD 基因外显子 8 和/或外显子 9 缺失的患者。 杜氏肌营养不良症 (DMD) 是最常见的儿童型肌营养不良症,通常发生在男孩身上。这是一种遗传性退行性疾病,会导致肌肉无力和肌肉组织损失,并随着时间的推移而恶化。平均预期寿命约为 27 岁。DMD 是由抗肌萎缩蛋白基因突变引起的,该突变导致肌萎缩蛋白水平低,而抗肌萎缩蛋白是增强肌肉纤维所必需的。Elevidys 旨在通过将编码功能性缩短抗肌萎缩蛋白(称为 Elevidys 微抗肌萎缩蛋白)的基因输送到肌肉组织中来治疗 DMD 的根本原因。 4、Skysona 公司:蓝鸟生物 疾病:脑肾上腺白质营养不良症(CALD) 每次治疗:300 万美元 FDA 批准日期:2022 年 9 月 16 日 Skysona(elivaldogene autotemcel 或 eli-cel)基因疗法被批准为第一种减缓 4 至 17 岁早期活动性脑上腺脑白质营养不良 (CALD) 男孩神经功能障碍进展的治疗方法。Skysona 由患者自身的干细胞制成,并经过修饰以包含基因拷贝,以制造一种称为 ALDP(肾上腺脑白质营养不良蛋白)的功能性酶。Skysona 作为单次、一次性静脉内 (IV) 输注治疗给药,费用为 300 万美元。 脑肾上腺脑白质营养不良 (CALD) 是一种罕见的、遗传性的和致命的神经退行性疾病,主要发生在年轻男孩中(中位发病年龄 7 岁)。CALD 是由于 ABCD1 基因突变而发生的,该突变阻止了 ALDP 酶的产生。这可以防止非常长链脂肪酸的分解,从而导致神经周围的鞘(髓鞘)被破坏。CALD 导致沟通能力丧失、皮质盲、需要管饲、完全失禁、依赖轮椅或完全丧失自主运动。近一半未接受治疗的患者在症状出现后 5 年内死亡。 5、Zynteglo 公司:蓝鸟生物 疾病:输血依赖型地中海贫血 每次治疗:280 万美元 FDA 批准日期:2022 年 8月 17日 Zynteglo(betibeglogene autotemcel 或 beti-cel)是一种慢病毒载体 (LVV) 基因疗法,被批准用于治疗需要定期输注红细胞 (RBC) 的成人或儿童 β-地中海贫血患者。Zynteglo 是专门为每位患者用自己的干细胞制成的,以一次性单剂量静脉内 (IV) 输注的形式给药,费用为 280 万美元。 β-地中海贫血是一种罕见的遗传性血液病,可导致严重贫血和终生依赖红细胞输注,患者通常每 2 至 5 周经历一次漫长的过程。Zynteglo 的工作原理是将 β-珠蛋白基因(βA-T87Q-珠蛋白基因)的修饰形式的功能拷贝添加到患者自身的造血(血液)干细胞中。该基因被添加到患者体外(离体)的细胞中,然后注入患者体内。这可能导致总血红蛋白水平正常或接近正常水平,并且可以消除定期输注红细胞的需要。 6、Zolgensma 公司:诺华 疾病:脊髓性肌萎缩症 每次治疗:212.5万美元 FDA 批准日期:2019 年 5 月 24 日 Zolgensma(通用名:onasemnogene abeparvovec-xioi)是一种挽救生命的基因疗法,被批准用于治疗 2 岁以下儿科患者的脊髓性肌萎缩症 (SMA)。Zolgensma 接受一次性、单剂量、静脉内 (IV) 输注治疗,批准总费用为 212.5 万美元。它通过替换有缺陷或缺失的存活运动神经元 1 (SMN1) 基因来治疗 SMA 的根本原因并阻止疾病进展。它被认为可能治愈。 脊髓性肌萎缩症 (SMA) 是一种罕见的遗传性运动神经元疾病,会导致呼吸、抬头和吞咽问题,由SMNA1基因突变引起。大多数 SMA 儿童由于无法呼吸(呼吸衰竭)而无法活过童年早期。美国每年约有 500 名婴儿出生时患有 SMA。佐尔根斯玛使用腺相关病毒作为载体,将人类SMN基因的功能拷贝送入靶运动神经元细胞,从而产生正常的SMN蛋白,支持肌肉功能。 7、Myalept 公司:奇爱制药 疾病:脂肪代谢障碍 / 瘦素缺乏症 每年费用:130万美元 FDA 批准日期:2014 年 2 月 24 日 多年来,瘦素缺乏症药物 Myalept 在全球最昂贵药物年度排名中一直处于领先地位。直到基因疗法出现。 Myalept(注射用美曲普汀)被 FDA 批准作为替代疗法,用于治疗先天性或获得性全身性脂肪代谢障碍患者瘦素缺乏症并发症。脂肪代谢障碍可以通过基因遗传,也可以在没有已知原因的情况下获得。 脂肪代谢障碍是一种罕见的疾病,会影响身体储存和使用脂肪的方式。脂肪可能会积聚在不该存在的地方,例如血液和器官。全身性脂肪代谢障碍患者经常出现严重的胰岛素抵抗、糖尿病或高水平的甘油三酯(高甘油三酯血症),这可能导致胰腺炎症。 Myalept 以皮下(皮下)注射的形式给药,每天一次,可以教患者在家中自行服药。一瓶 11.3 毫克的小瓶售价约为 6,188 美元,剂量基于重量。例如,患者每月可能使用大约 18 个小瓶,因此每年的药物成本可能超过 130 万美元。 8、Danyelza 公司:Y-mAb Therapeutics 病症:神经母细胞瘤 每年费用:120 万美元 FDA 批准日期:2020 年 11 月 25 日 Danyelza (naxitamab-gqgk) 40 mg/10 mL 被批准用于治疗患有骨骼或骨髓中高危神经母细胞瘤的成人和 1 岁及以上的儿童,与粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 联合使用,他们已证明对先前的治疗有部分反应、轻微反应或疾病稳定。它用于已经进展或对治疗反应不完全的患者。 神经母细胞瘤是一种实体瘤,发生在大脑外的神经系统中,最常见于婴幼儿。这些肿瘤细胞可以扩散(转移)到身体的其他部位,例如骨骼或骨髓。有些肿瘤可以治疗,但大多数肿瘤非常具有侵袭性。 Danyelza 被归类为 GD2 结合单克隆抗体免疫疗法。它的工作原理是附着在肿瘤细胞上并向免疫系统发送信号以杀死癌症。Danyelza 在一周内(每 28 天周期)作为静脉内 (IV) 输注在门诊(如诊所)对患者进行 3 次给药。治疗周期每 4 周重复一次,直到完全或部分缓解,然后每 4 周增加 5 个周期。后续周期可每 8 周重复一次。每个 40 mg/10 mL (4 mg/mL) 单瓶的成本约为 24,300 美元。治疗时间长短取决于反应,剂量基于体重,因此很难估计确切的成本。例如,如果患者使用 48 瓶药物,则每年的药物成本约为 120 万美元。Danyelza 还与 GM-CSF 结合使用,以帮助您的身体产生某些血细胞,这些血细胞有助于对抗癌症并帮助预防感染,这会增加治疗成本。 9、Zokinvy 公司:Eiger BioPharmaceuticals 艾格生物制药公司 病症:哈钦森-吉尔福德早衰综合征和加工缺陷型早衰层状病变 每年费用:120万美元 FDA 批准日期:2020 年 11 月 20 日 Zokinvy(lonafarnib)用于治疗Hutchinson-Gilford早衰综合症(HGPS或Progeria)和加工缺陷型早衰样板纤病(PL)。Zokinvy 适用于体表面积 (BSA) 为 0.39 m (2) 及以上的 12 个月及以上的成人和儿童患者。Zokinvy 为遗传性早衰疾病患者提供生存益处。 早衰症和早衰样板层蛋白病是非常罕见的遗传性过早衰老疾病,会加速年轻患者的死亡。未经治疗的早衰症儿童平均年龄为 14.5 岁死于心脏病。在美国,已知大约有 20 名儿童和年轻人患有这种疾病。 Zokinvy 是一种疾病调节剂,可阻断有缺陷的法尼基化蛋白的积累。Zokinvy 剂量基于体表面积 (BSA),每天两次以胶囊形式给药,早晚饭服用。Zokinvy 的成本约为 26,000 毫克胶囊中的 30 粒和 39,000 毫克胶囊中的 30 美元。例如,一名患者每天服用 4 粒 50 毫克胶囊,每年的费用约为 120 万美元。 10、Kimmtrak 公司:免疫核心 疾病:葡萄膜黑色素瘤 每年费用:110万美元 FDA 批准日期:2022 年 1 月 25 日 2022 年 1 月,FDA 批准了 Kimmtrak (tebentafusp-tebn),这是一种免疫疗法,用于治疗 HLA-A*02:01 阳性的葡萄膜黑色素瘤成人患者,这些患者已经扩散到身体的其他部位或无法通过手术切除。Kimmtrak 通过附着在 HLA-A*02:01 / gp100 复合物上起作用,HLA-A*02:01 / gp100 复合物是一种通常在葡萄膜黑色素瘤癌细胞中表达的谱系抗原。免疫疗法与您自己的免疫系统一起作用,帮助您的身体对抗癌症。Kimmtrak 是第一个获得 FDA 批准的 T 细胞受体 (TCR) 疗法。 葡萄膜黑色素瘤是一种罕见的侵袭性眼癌。高达 50% 的葡萄膜黑色素瘤患者最终会在身体的其他部位发展为癌症。 推荐剂量为第 1 天 20 微克静脉内 (IV) 输注,然后第 8 天 30 微克静脉输注,第 15 天 68 微克静脉输注,此后每周 68 微克静脉输注。Kimmtrak 静脉注射液 (100 mcg/0.5 mL) 的费用约为 20,764 美元,或每年的费用约为 110 万美元。患者通常接受治疗,直到出现不可接受的毒性或疾病进展。
2024-09-12
合成人工代谢酶实现肿瘤特异性代谢治疗
日益增多的证据表明,代谢紊乱与一系列难治性疾病有关,如癌症、糖尿病及心脏病等。Warburg效应的发现为肿瘤微环境(TME)中的代谢调控策略提供了新的视角,这一策略在精确治疗癌症方面展现出巨大的潜力。与传统的针对特定细胞群体的方法不同,代谢靶向手段,如针对糖、嘌呤、天冬氨酸、谷氨酰胺或脂质的代谢途径,对于管理癌症等代谢活跃疾病的复杂病理过程具有显著的治疗效果。 在小分子和寡核苷酸代谢调节剂的研究和临床应用方面,已经实现了针对特定代谢途径的靶向治疗,并在癌症治疗领域取得了显著的进展。尽管如此,现有的代谢调节剂往往缺乏对肿瘤细胞的特异性,其疗效常常受限于意外的脱靶效应和短暂的作用时间。 在生物系统中,酶作为先天调节剂,能够以极高的特异性和亲和力,通过极少的辅助步骤迅速将底物转化为目标产物,对于复杂的肿瘤微环境(TME)中的代谢变化起着至关重要的协调作用。 近日,上海交通大学变革性分子前沿科学中心凌代舜教授团队和上海交通大学医学院李方园教授团队合作,在《Nature Nanotechnology》发表题为“An artificial metabzyme for tumour-cell-specific metabolic therapy”的研究论文。 相关论文 该研究首次开发了一种具有代谢酶活性的“人工代谢酶”——FeMoO(4)纳米催化剂,它拥有双活性中心:铁(Fe(2+))和四面体钼(Mo(4+)),模仿了典型代谢酶黄嘌呤氧化酶(XOR)的特征结构。通过空间动态代谢组学技术,结合对肿瘤特异性代谢物的深入分析,研究揭示了FeMoO(4)代谢酶催化肿瘤中丰富的黄嘌呤转化为尿酸,并通过后续的代谢重调与免疫细胞的相互作用,精准激活了针对肿瘤的免疫反应,开辟了一种新的癌症治疗策略。 这项研究为癌症治疗领域带来了突破性的新思路,通过人工代谢酶的作用,肿瘤细胞的代谢途径被重新编码,使其能够自我调节并与免疫细胞相互作用,专门针对肿瘤细胞的代谢进行治疗。 FeMoO(4)人工代谢酶用于肿瘤细胞特异性代谢激活免疫治疗 类酶纳米催化剂(也称为纳米酶)的出现具有变革性潜力,它有望突破天然酶所面临的成本、稳定性和保存难度等局限。数十年来,纳米酶技术迅猛发展,涌现出众多创新材料,它们被设计来复现氧化还原酶、水解酶、裂合酶等天然酶的功能。尽管如此,开发出具备多金属代谢酶特性的合成纳米酶依然是一个技术挑战。在原子层面,实现高异质金属原子的负载与活性位点在金属氧化物基质中的有效整合,仍是一个亟待攻克的难题。 本项研究受到经典代谢催化剂——黄嘌呤氧化酶(XOR)的启发,该酶负责将黄嘌呤(Xanthine)转化为尿酸(UA),其催化机制依赖于铁(Fe)和四价钼(Mo)的双重辅因子。XOR的活性与多种癌症的不良预后紧密相关,尤其是那些XOR表达水平较低的癌症,这强调了它在炎症反应中的关键作用。揭示了黄嘌呤衍生物的免疫抑制特性以及尿酸在促进抗肿瘤免疫反应中的重要作用,这进一步凸显了XOR在本研究中的重要性。 基于这些发现,研究团队设计了一种创新的合成方法(腐蚀-吸附-固定),该方法通过将铁原子以精确的化学计量比掺入到MoO(3-x)催化剂中,并促使原子重新排列形成四面体催化结构,成功合成了FeMoO(4)纳米催化剂。这种人工代谢酶的设计,不仅复制了XOR的Fe(2+)和Mo(4+)活性中心,而且实现了对XOR催化过程的完美模拟。 FeMoO(4)人工代谢酶的设计与构建 在FeMoO(4)代谢酶抵达那些XOR活性不足且黄嘌呤浓度升高的肿瘤细胞时,它能够高效地催化黄嘌呤转化为大量的尿酸(UA),并立即激活巨噬细胞释放炎症性细胞因子,如IL-1β,这进一步促进了具有免疫激活功能的M1型巨噬细胞的分化,以及树突状细胞和T细胞等其他免疫细胞的活化。 值得注意的是,这种代谢调节促进了免疫细胞间的代谢串扰(Crosstalk),影响了它们的功能和决策过程,进而对肿瘤细胞发起了联合攻击——这种协同作用推动了靶向肿瘤细胞的特异性代谢治疗。 FeMoO(4)人工代谢酶的理化性质分析 鉴于肿瘤内PD-1/PD-L1表达上调,FeMoO(4)代谢酶展现出与免疫检查点抑制剂协同作用的潜力。实验数据表明,FeMoO(4)代谢酶在抑制B16黑色素瘤细胞增殖方面表现出显著效果,并且当与PD-1抗体联合应用时,治疗效果更为显著,有效减缓了肿瘤的增长速度,并显著延长了小鼠的存活时间。FeMoO(4)代谢酶有望逆转肿瘤微环境(TME)中的免疫抑制状态,并增强肿瘤细胞表面PD-L1的表达,为提升免疫检查点抑制剂的疗效提供了一种潜在的替代治疗策略。 FeMoO(4)人工代谢酶介导肿瘤特异性代谢激活免疫治疗 本项研究专注于模仿天然代谢酶的人工合成以及调节肿瘤-免疫细胞之间的相互作用。通过设计合成能够精准调控特定代谢途径和产物的人工代谢酶,提出了一种创新的代谢免疫激活策略。这种策略为与代谢紊乱相关的一系列严重疾病—如癌症、心脏病、痛风和糖尿病等—提供了一种依托于人工代谢酶的全新免疫代谢调节方法,引领了由化学生物学推动的精确代谢治疗的新纪元。 前衍可提供产品 12650-88-3 溶菌酶(蛋清) 9001-22-3 β-葡糖苷酶 9015-68-3 门冬酰胺酶
2024-09-04
六起易制爆、危化品不合规处罚案例
未经许可报备无证经营危险化学品 7人因非法经营罪获刑 2022年,广东省广州市南沙区人民法院审结一宗非法经营危险化学品案,以非法经营罪分别判处被告人丘某娣等7人有期徒刑四年至一年六个月,并处罚金,其中被判处缓刑的被告人李某清等4人在缓刑考验期内禁止从事危险化学品贸易、运输等经营活动。 【简要案情】 法院经审理查明,被告人丘某娣、李某清作为登记股东,于2014年8月依法成立英德市某蓬化工公司并在英德市取得经营许可,该公司住所地为广东省英德市东华镇某村、性质为自然人投资的有限责任公司,被告人丘某娣是实际控制人、法定代表人。 该公司的经营范围包括贸易经营硝酸钠、硝酸钾、超氧化钠、超氧化钾、高锰酸钾等易制爆物,贸易经营丙酮、甲苯、硫酸、乙醇等危险化学品。截至案发当日,该公司上述危化品经营许可证、易制爆、易制毒化学品经营备案证均在有效期内。 2019年10月前,被告人丘某娣、李某清未经许可、报备,在广州市白云区设立英德市某蓬化工公司经营点从事危险化学品等的经营。该经营点设立后,无登记,未取得法人资格,持续从事违法犯罪行为。 2019年10月起,被告人何某洲、黄某某、黄某兴、江某成、黄某坚陆续加入某蓬化工公司广州市白云区非法经营点并于2020年10月1日与被告人丘某娣、李某清签署合作协议,约定将该非法经营点作为合作项目的合作内容、股权分配情况、分工情况等。此后各被告人在广州市白云区继续租赁办公场所和仓库,以某蓬化工公司名义对外销售包括无水乙醇、丙酮等在内的危险化学品(部分危险化学品同时又属于易制爆、易制毒化学品)。相关货物销售去向包括深圳市、广州市等。 经查明,何某洲、黄某某、黄某兴、江某成、黄某坚加入后,上述非法经营点非法经营危险化学品的金额共计为1744954.74元。 【裁判结果】 法院审理后认为,本案中各被告人所违反的《危险化学品安全管理条例》等规定,属国务院制定的行政法规,应认定为“违反国家规定”。且本案各被告人非法经营危险化学品的数额为1744954.74元(含未销售部分),已达“情节严重”标准。同时,法律、行政法规对危险化学品的销售、储存、运输均有规定,包括:卖方要经许可,买方需要资质,买卖要报备,存储、运输有特殊要求等。因此,本案涉及的危险化学品属于法律、法规规定的限制买卖的物品。综上,各被告人违反国家规定,非法经营危险化学品,扰乱了市场秩序,情节严重,构成非法经营罪。综合7名被告人的犯罪事实、犯罪的性质、情节、危害后果及认罪态度,法院依法作出判决。以非法经营罪分别判处被告人丘某娣等7人有期徒刑四年至一年六个月,并处罚金,其中被判处缓刑的被告人李某清等4人在缓刑考验期内禁止从事危险化学品贸易、运输等经营活动。 【法官提醒】 危险化学品多数具有毒害、腐蚀、爆炸、助燃等性质。一旦处置不当,极有可能给人民群众的生命财产安全以及社会公共安全带来危险。因此,我国对危险化学品的经营(包括运输、仓储、买卖等)实行许可制度。经营危险化学品的企业应当依照有关法律法规,取得危险化学品经营许可证。取得许可证后,应该按许可的危化品种类、等级、地域依法经营,不得将许可证出借、出租或跨地域经营。否则将依法承担行政责任,构成犯罪的,将追究刑事责任。 江苏省苏州市姑苏区应急管理局查处苏州市东吴玻璃仪器有限公司在电商平台违法售卖危险化学品案 2023年2月27日,江苏省苏州市姑苏区应急管理局收到北京经济技术开发区管理委员会《举报情况移送函》,反映辖区苏州市东吴玻璃仪器有限公司涉嫌在电商平台违法销售危险化学品。经查,该公司在电商平台注册“东吴工业品”专营店,于2022年3月发布了商品氯化钡(商品编号:10041757258151)的销售信息。氯化钡上架期间,无违法销售记录、无违法所得。氯化钡为《危险化学品名录(2015版)》列明的危险化学品,并且不在该公司危险化学品经营许可证“许可范围”内。依据《危险化学品安全管理条例》第七十七条第三款的规定,对该公司处以人民币107500元罚款的行政处罚。 安徽省合肥市公安局查处健坤化工有限公司购买易制爆危险化学品未进行备案案 2023年4月,合肥市公安局蜀山分局利用安徽省危险化学品治安管理信息系统,发现合肥健坤化工有限公司购买易制爆危险化学品入库备案不及时(超过5天)的情况,且信息预警6次,该公司仍未采取任何措施。该公司的行为违反了《危险化学品安全管理条例》第四十一条第二款的规定,依据《危险化学品安全管理条例》第八十一条第一款第五项的规定,合肥市公安局蜀山分局依法对该公司处以5000元罚款的行政处罚。 河南省开封市杞县应急管理局查处无证销售危险化学品案 2023年4月13日,开封市杞县应急管理局执法人员发现有人在某社交平台上视频宣传利用流动油罐车销售柴油。经核查,位于杞县某商砼站院内停放一辆储存危险化学品(柴油)的油罐车,现场测量油罐内还有柴油300L。柳某在社交平台上看到厂家的宣传广告,厂家声称销售合法的加油车、手续齐全。于是柳某买了一辆,并利用社交平台销售柴油,购油者通过社交平台下单、支付或现金支付。当事人柳某未经许可、无证经营危险化学品,该行为违反了《危险化学品安全管理条例》第三十三条第一款的规定,依据《危险化学品安全管理条例》第七十七条第三款的规定,杞县应急管理局责令其停止非法经营行为,没收柴油300L及违法所得9860元,并处以人民币100500元罚款的行政处罚。 塞隆化工产品销售有限公司自营网站发布危险化学品信息被罚 2023年5月4日,淮南市市场监管局发现淮南市赛隆化工产品销售有限公司在其自建网站展示、发布氨水、硝酸、双氧水等危险化学品信息,但其网站公示的营业执照经营范围不含危险化学品经营,也未公示其危险化学品经营许可证,未标明个人或单位购买危险化学品所需要具备的资质和条件。6月25日,淮南市市场监管局依据《网络交易监督管理办法》《电子商务法》,予以当事人罚款1000元的行政处罚。 浙江省杭州市余杭区市场监管局查处涉危险化学品的虚假广告案 2023年5月16日,余杭区市场监管局根据有关线索,对当事人刘某开设的网店“鑫盛贵金属”进行调查。经查,当事人自2022年12月8日起在电商平台上发布“稀硫酸溶液60%1000毫升稀硫酸标准溶液中小学化学实验用实验室”的商品及相应广告。经检测,该商品硫酸根离子含量小于1%,与网店描述(60%稀硫酸)不一致。网页页面宣传“60%稀硫酸”目的为便于获取商品流量,实际商品为自制油污清洁剂。至2023年5月16日商品下架,该商品共销售5492件。当事人的行为违反了《中华人民共和国广告法》第二十八条第二款第(二)项的规定,构成虚假广告。依据《中华人民共和国广告法》第五十五条第一款的规定,余杭区市场监管局对当事人发布虚假广告行为处以1万元罚款的行政处罚。
2024-08-28
蚊子为何偏爱某些人?如何阻断蚊媒病毒传播?
自然界中存在数百种蚊媒病毒,它们通过蚊虫传播给人类和动物,引发包括病毒性脑炎、脑膜炎和出血热在内的严重疾病。近二十年来,以登革病毒、寨卡病毒、基孔肯亚病毒、西尼罗病毒为代表的新发及再发蚊媒病毒在全世界流行,每年可导致数十亿人感染、数十万人死亡。 目前,大多数烈性蚊媒病毒缺乏有效的疫苗和治疗药物。科学界迫切需要深入理解这些病毒在自然界中的传播机制,并开发创新的防控策略,以防止它们在全球范围内的进一步传播。 2022年6月30日,清华大学教授程功,一位有16年蚊虫研究经验的专家,在《Cell》(细胞) 上发表了重要研究,题为“A volatile from the skin microbiota of flavivirus-infected hosts promotes mosquito attractiveness”(皮肤共生微生物来源的一种气味挥发物促进黄病毒感染宿主吸引蚊虫)。 蚊媒病毒在宿主与蚊虫之间传播循环。在病毒传播循环中,蚊虫需要寻找、定位并叮咬感染的人或动物,取食带有病毒的血液。随后,蚊虫才能具备携带并快速传播病毒的能力。如果蚊虫叮咬非感染者,则不会有效获取病毒感染,病毒的传播循环则被中断。 蚊媒病毒“宿主-蚊”传播循环 观察发现,在蚊媒病毒暴发流行初期,人群中的感染者比例并不高 (仅千分之一、甚至更低)。而蚊虫却能选择人群中的感染者进行叮咬,从而加速病毒传播,引起疫情暴发。可见,蚊虫如何有效定位感染宿主并获取病毒是病毒完成“宿主-蚊”传播循环的主要限速步骤。这引出一个长期以来有待解决的科学问题:蚊虫如何在茫茫人海中定位感染者?如能弄清这个问题,就能解释蚊媒病毒在自然界快速传播的原因,进一步找到简便有效方法遏制病毒快速传播。 本研究中,程功团队使用了两套经典的行为学装置 (三笼嗅觉测定装置、双臂嗅觉测定装置),观察到登革病毒和寨卡病毒感染的小鼠对埃及伊蚊及白纹伊蚊具有显著的吸引力。接着,研究人员分析了感染病毒的小鼠的体温、二氧化碳排放和挥发性气味,发现宿主气味的改变是造成感染宿主吸引蚊虫的决定性因素。进一步研究发现,在蚊媒病毒的感染之后,实验鼠能够大量释放挥发性小分子—苯乙酮 (Acetophenone),这种物质能够有效地激活蚊虫的嗅觉神经系统,从而增强蚊虫对感染小鼠的行为趋向。 进一步的实验中,研究人员采集了登革热患者及健康志愿者的气味样本,结果发现,登革热患者的气味对埃及伊蚊具有更强的吸引效果。并且,登革热患者的气味中,苯乙酮含量也显著高于健康志愿者。研究人员将不同浓度的苯乙酮涂抹于人体手臂进行蚊虫行为学验证,发现增加人体气味中的苯乙酮含量能显著吸引蚊虫。以上试验说明,登革热患者由于释放大量苯乙酮改变自身气味,大幅提高了对蚊虫的吸引力,吸引蚊虫叮咬,加速病毒传播。 研究人员发现,人体或动物释放的苯乙酮主要来源于体表的皮肤共生微生物,这是一种典型的细菌代谢产物。一旦去除皮肤共生微生物后,感染小鼠便不再对蚊虫具有更强的吸引力。进一步研究显示,登革病毒及寨卡病毒感染可导致宿主皮肤表面芽孢杆菌属 (Bacillus spp.) 细菌的丰度明显上升,而这些细菌具有代谢产生大量苯乙酮的能力。至此,研究人员揭示了蚊媒病毒感染者吸引蚊虫叮咬的原因:病毒感染提高了人体皮肤中特定细菌的比例,显著增强了感染者释放苯乙酮的能力,从而明显提升了蚊虫对感染宿主的行为趋向。 随后,研究者对对感染和未感染病毒的小鼠皮肤组织进行转录组测序 (RNA-Seq) 分析,发现感染宿主的皮肤中抵抗素样分子-alpha (Resistin-like molecule-alpha, RELM-alpha) 基因达显著降低 (20-100倍,RNA-Seq)。RELM-alpha作为一种抗菌肽,与抵抗素(Resistin,RETN) 为同源蛋白,在人类及哺乳动物的皮肤角质细胞及皮脂腺细胞中特异表达,是决定宿主皮肤微生物稳态的主要免疫因子。进一步研究结果显示,RELM-alpha及RETN可高效抑制多种皮肤芽孢杆菌的增殖。以上研究说明,登革病毒和寨卡病毒感染可通过抑制宿主皮肤中RELM-alpha/RETN的表达,导致原本被抑制的皮肤芽孢杆菌过量增殖,而引起感染宿主的苯乙酮释放量升高。 前期研究结果显示,RELM-alpha/RETN的表达受到视黄酸受体信号通路 (Retinoic Acid Receptor signaling pathway, RAR signaling pathway) 的调控。通过向动物饲喂维生素A衍生物,可以激活RAR信号通路,诱导RELM-alpha/RETN的表达。本研究结果显示,向感染登革热和寨卡病毒的小鼠体内饲喂一种维生素A衍生物—异维甲酸 (isotretinoin,一种临床广泛使用的皮肤病治疗药物),能有效恢复感染小鼠皮肤中RELM-alpha的表达,达到抑制感染宿主皮肤中芽孢杆菌的增殖,减少感染宿主释放苯乙酮的目的。因此,感染宿主口服异维甲酸后,蚊虫将无法通过宿主的苯乙酮来定位和识别感染宿主,从而阻断病毒的传播循环。 基于这些发现,研究者提出了一种新的蚊媒病毒防治思路:通过调控人体气味,阻断蚊媒病毒的快速传播。考虑到在蚊媒病毒传染病的早期阶段,感染者在人群中的比例仅有千分之一、甚至更低,研究团队推断,在感染者摄入维生素A类药物后,蚊虫将无法通过苯乙酮的气味区分感染者和非感染者,这将显著降低蚊虫吸食感染者血液并传播感染的可能性,从而阻碍蚊媒病毒在自然界中高效建立“宿主-蚊”的传播链。据此,研究团队提出一种新的蚊媒病毒传染病防控策略:在登革热和寨卡热等蚊媒病毒流行的疫区,广泛为感染者补充维生素A或相关药物,重塑感染者皮肤微生物挥发的气味,显著降低蚊媒病毒的传播效率,有效防止蚊虫携带并传播病毒。 但是,当程功团队尝试把这一策略应用于大众时,他们才发现这并不可行。“在人群中推广一种药物,尤其是让大家未雨绸缪地吃药,需要很长一段时间的过渡期。然而,传染病发展之快,光靠药物防治,很难抑制住。” 因此,程功决定走出实验室,到自然界中探寻答案。并于2024年4月19日,在《Science 》(科学)上发表了新的研究论文,题为“A naturally isolated symbiotic bacterium suppresses flavivirus transmission by Aedes mosquitoes(一种天然定植的伊蚊肠道共生菌阻断蚊媒黄病毒传播)”。 沿着蚊媒传染病高发的云南边境,程功团队走过了7个城市和地区,原本计划实地考察登革热的发病情况,却意外发现了一种特殊的现象:相邻的两个地区,发病率却大有差别,“比如,在云南文山州的麻栗坡县,旁边的地区登革热疫情很严重,但这个地方只有零星几个病例,而且控制得很好,这是为什么?难道是受环境影响?”程功说,科研的开端往往始于一个发现、一个猜想。 2020年5月,程功在云南省成立专家工作站,接下来的3年里,科研人员在云南边境地区捕捉了数千只野外雌性伊蚊,通过研究它们的肠道微生物,分离出55株蚊虫肠道共生菌,判断环境的差别并进行功能筛选。研究显示,在常见的白纹伊蚊及埃及伊蚊的肠道中定植Rosenbergiella_YN46菌,可显著抑制蚊虫通过叮咬吸血感染登革病毒及寨卡病毒。Rosenbergiella_YN46菌是一种能决定蚊虫对病毒易感性的关键肠道共生菌,通过分泌一种葡萄糖脱氢酶将吸血蚊虫肠道环境快速酸化 (pH≈6.0),导致蚊虫肠道微环境重塑,大幅降低蚊虫对病毒易感性。它在自然界中广泛存在,与植物汁液和花蜜有关,在非登革热流行地区的蚊虫肠道中有很高的定植率,而在登革热流行地区则相反。 Rosenbergiella_YN46菌在自然界中的分布定植 与云南地区登革热流行地区特异性存在高度负相关 为将科研成果应用于实际,程功团队在西双版纳傣族自治州勐腊县设计了一个现场干预实验。研究结果表明,通过向蚊虫孳生水体中加入Rosenbergiella_YN46菌进行环境干预,孵化出的疫区蚊虫感染登革病毒的比例大幅下降。 在孳生地水体中进行Rosenbergiella_YN46环境干预可有效降低蚊虫携带并传播病毒 “相较于传统蚊媒病毒防控手段,研制Rosenbergiella_YN46菌成本低、效率高、安全系数高。”程功介绍,他们已经在一个村落进行了大规模现场干预实验,一旦取得成功,将扩大实验范围,一步步实现共生菌环境干预策略的落地。 前衍可提供的部分实验材料,更多请咨询客服 98-86-2 苯乙酮 4759-48-2 异维 A 酸 68-26-8 维生素A
2024-08-21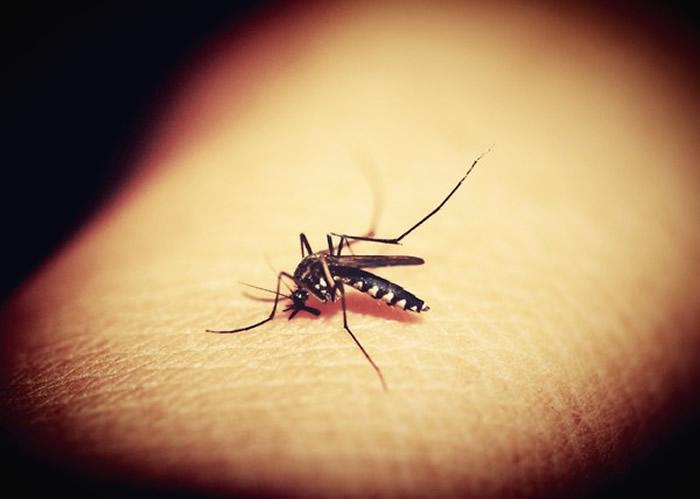
我国科研团队新纪录:有机小分子催化达百万次
近期,西湖大学副校长邓力的研究小组在《JACS(美国化学会志)》发表了一篇题为《Practical Synthesis of Chiral α-Aminophosphonates with Weak Bonding Organocatalysis at ppm Loading(ppm级不对称弱键有机催化合成α-氨基膦酸酯)》的封面文章。该团队借鉴酶的催化机制,以弱键作为主要驱动力开发了一种高效的催化方法。 1个催化剂分子,完成100万次催化,其转化数(TON)达到1:1000000。此项成就不仅刷新了有机小分子催化领域的最高记录,还使其催化效能与自然界中的酶相提并论。 地球生命的能量来自催化过程,生命活动本身也依赖酶的高效催化。例如,在非酸非碱环境下,一个蛋白质断裂其一半的肽键大约需要500年,而酶解开一个肽键仅需几纳秒。 上世纪末,有机小分子催化开始崭露头角。与传统金属有机催化剂相比,这种催化方式具有显著的优势,包括对氧气和水的不敏感性、原料的易获取性、成本低、易于储存、较低的毒性等。其中,不对称有机催化通过精确控制反应过程,确保产物只在一种空间构型上发生,从而仅产生需要的产物。不对称有机催化主要有共价催化和弱键催化两种模式。 低催化效率是限制有机催化领域进步的主要障碍,也是该领域面临的一大科学挑战。探索是否能够借鉴生物酶的催化机制,开发出新一代有机小分子催化剂,以实现与酶催化相媲美的效率,同时保持对底物的广泛适用性,是有机催化领域理论发展和在合成化学中应用的关键问题。邓力团队专注于弱键催化。这是因为在自然界中,包括人体中的酶,常通过多种弱键协同作用来激发催化反应,并精确控制反应结果。 邓力团队研发手性季铵盐有机小分子催化剂,成功开创了一种最高效实用的α-氨基膦酸衍生物不对称合成新方法,高对映选择性地合成了一系列手性氨基膦酸酯。特别值得关注的是,该催化剂在极低的载量(0.8-50 ppm,百万分之一)下,能够合成多种α-烷基手性氨基膦酸酯,并且其转换数可达到20000以上,催化效率与生物酶相媲美。尤其是当使用α-甲基亚胺膦酸酯作为底物时,其转化数超过了百万,刷新了不对称有机催化领域的纪录。 这种有机小分子催化物具有比酶类更广泛的底物适应性,同时其分子量显著低于酶,仅为酶的百分之一或更低。鉴于其改变了科学界对小分子催化剂和生物酶的传统认知,研究团队将其命名为“小分子酶”。 前衍能够提供的部分有机催化剂和酶,更多相关化合物请咨询客服 130-95-0 金鸡纳碱 147-85-3 L-脯氨酸 32503-27-8 四丁基硫酸氢铵 9000-90-2 α-淀粉酶 9001-00-7 菠萝蛋白酶 9032-75-1 果胶酶
2024-08-15
《Nature》:复旦发现新型高温超导体
超导体材料,在特定临界温度之下,电阻降为零且展现出完全抗磁性,从而能够无损耗地传导电流,这些特性使其在电力传输和储能、医学成像、磁悬浮列车、量子计算等领域具有广泛的应用前景。由于其潜在的广泛应用,超导体的研究一直是科学界的热点,至今已经有多位科学家因在超导领域的贡献而荣获诺贝尔奖。7月17日,Nature报道了复旦大学的一项突破性发现,该校物理学系赵俊教授团队利用高压光学浮区技术培育出了三层镍氧化物La4Ni3O10。通过高质量单晶样品,研究团队证实了镍氧化物中具有压力诱导的体超导电性(bulk superconductivity),且其超导体积分数达到86%。此外,研究还发现该类材料呈现出奇异金属和独特的层间耦合行为,为深入理解高温超导机理提供了新的视角和平台。 1911年,荷兰物理学家海克·卡末林·昂内斯(Heike Kamerlingh Onnes)首次在在汞(Hg)中观察到了超导现象,这一发现发生在他将汞冷却到约4 K(“K”为热力学温度单位“开尔文”,4 K=-269.15℃)时,此时汞的电阻突然消失变为0。此后很长一段时间内,科学界普遍认为,只有汞、铝等金属及其简单合金,在极低的温度条件下,才能展现出超导性。 直到1986年,约翰内斯·贝德诺尔茨(Johannes Georg Bednorz)和卡尔·亚历山大·米勒(Karl Alexander Müller)在镧钡铜氧化物(La-Ba-Cu-O)中发现了高温超导现象,且临界温度可以高达30 K(-243.15°C)。此后,包括中国科学家在内的多国科学家将其超导临界温度提升至液氮温区(77 K,-196.15°C),甚至超过了130 K(-143.15°C)。 高温超导现象的发现,颠覆了人们对于超导现象仅存于极低温的传统观念。全球的科学家们对这一现象进行了广泛而深入的探索,但经过近四十年努力,其形成机理仍是未解之谜。 镍在元素周期表中紧邻铜,镍氧化物被视作高温超导电性实现的关键候选材料之一。然而,历经数十年的探索,科学家们发现在镍氧化物中实现超导电性的条件十分苛刻。 2019年,具有无限层NiO2面的Nd0.8Sr0.2NiO2体系被发现具有超导电性,其转变温度介于5 K(-268.15°C )至15 K(-258.15°C )之间。然而,这种超导性仅在薄膜样品中被观察到,而块状材料则未能发现。 2023年,中国科学家在具有双层NiO2面结构的镍氧化物La3Ni2O7中,发现了压力诱导的高温超导电性,其临界温度高达80 K(-193.15°C ),将镍氧化物的超导转变温度提高到了液氮温区。然而,这种材料的超导体积分数较低,容易表现出丝状超导现象(filamentary superconductivity),难以形成体超导电性。因此,寻找新的超导体系,提高超导体积分数,实现体超导电性显得尤为关键。 在Nature此次发布的研究成果中,赵俊教授的团队通过高压光学浮区法成功合成了高质量的三层镍氧化物La4Ni3O10单晶样品。这些样品在超导临界温度下表现出了零电阻和完全抗磁性,即迈斯纳效应,其超导体积分数高达86%,这有力证实了镍氧化物的体超导特性。赵俊教授指出,“这个超导体积分数与铜氧化物高温超导体接近,毫无疑问证实了镍氧化物的体超导电性。”在69 GPa的压力下,这种三层镍氧化物La4Ni3O10单晶的超导临界温度达到了30 K(-243.15°C )。 未来,赵俊教授的团队计划继续深入高温超导领域的重大问题,研究不同体系高温超导体之间的内在联系和作用机制,以期理解和发现性能更优的高温超导材料。 前衍可以提供的部分材料,更多可以咨询平台客服 7439-97-6 汞 7440-02-0 镍 7440-50-8 铜 7727-37-9 液氮 12031-75-3 锂锰镍氧化物
2024-08-07
“AI+机器人”加速发现新材料
当今世界,人工智能(AI)无疑是一个备受瞩目的焦点,尤其是像ChatGPT这样的大型语言模型的出现,在全球范围内引发了广泛关注。AI在科研领域的应用日益增多,并且不断深入。2021年《科学》杂志社评选的十大“年度突破”,“AI预测蛋白质结构”就高居榜首(Science, 2021, 374, 1426)。此外,在化学和材料科学领域,AI近年来也取得了显著成就,例如,可以根据分子结构准确预测不同分子的气味(Science, 2023, 381, 999),在没有化学家输入的情况下分析催化反应动力学数据并阐明相应的机理类别(Nature, 2023, 613, 689),设计复杂天然产物的全合成路线(Nature, 2020, 588, 83),为有机反应筛选最佳反应条件(Science, 2023, 381, 965),基于结构预测分子的抗菌活性(Cell, 2020, 180, 688)等。更令人瞩目的是,AI与机器人技术的结合,已经成为实验室的新新成员(Nature, 2020, 583, 237)。这些智能机器人不仅具备灵活的四肢,而且能够全天候工作,每天进行超过20小时的实验。 新材料的发现是一项耗时耗力的工作,正如爱迪生在发明电灯泡的过程中,试验了成千上万种灯丝材料。传统的试错法在寻找新材料时成本极高,这严重制约了新材料的迅速发现。然而,近年来,融合了机器人技术和主动学习策略的自动化探索模式应运而生,得益于人工智能(AI)结合机器人技术以及深度学习在多个领域的突破性进展,它们在材料科学的研究中扮演了关键角色。 谷歌DeepMind的研究团队在《自然》上发表了题为Scaling deep learning for materials discovery(Nature, 2023,624, 80)的重磅文章,深入探讨了如何利用深度学习技术显著加速新材料的发现过程。他们采用的技术名为“材料探索图网络(graph networks for materials exploration, GNoME)”,已经成功预测了220万种新材料的结构,这些结构中有许多并不符合人类科学家的化学“直觉”,已有超过700种在实验室中成功合成。 GNoME能够实现新材料的高效发现 预测材料的存在是一回事,而将它们实际制造出来并验证其应用潜力则是另一项挑战。在传统的人工操作实验室中,开发新材料是一个非常耗时的过程。劳伦斯伯克利国家实验室(LBL)研究者开发了一种名为A-Lab(Nature, 2023,624, 86)的自动化实验室平台,旨在缩短从计算筛选到实验合成新材料的时间差距。A-Lab利用计算模型、历史文献数据、机器学习和主动学习技术,结合机器人自动化,优化新材料的设计和合成流程。 A-Lab平台采用了一些由GNoME和"Materials Project"项目数据发现的材料,通过机器学习模型的训练,能够自主决定合成目标材料的最佳方法,并创建多达五种初始原材料的组合。每次实验完成后,A-Lab会根据实验结果对原材料组合进行调整。在短短17天内,A-Lab完成了355次实验,并成功合成了58种化合物中的41种,包括各种氧化物和磷酸盐。即使是合成失败的案例,也为改进材料筛选和合成设计技术提供了宝贵的反馈和建议,这些信息对于优化现有技术具有直接和实际的应用价值。 基于A-Lab进行自主材料发现 谷歌DeepMind和LBL的研究人员相信,这些新的AI工具能够显著加速能源、计算和其他众多领域的硬件技术进步。特别是新发现的材料种类,它们有望在电池技术、半导体芯片、陶瓷和电子产品等领域引发技术革命,并推动可持续性的进一步发展。传统上,新材料从被发现到实现商业化应用,往往需要数十年的时间。而AI结合机器人技术的应用,能够大大缩短这一周期,这无疑是一项巨大的技术飞跃。
2024-07-24
终结艾滋病?一年二针,100%有效预防
2024年6月20日,吉利德公司在其官方网站上宣布,在一项关键的3期PURPOSE 1临床试验中,每年仅需两次注射的长效药物lenacapavir在预防女性HIV感染上显示出100%的有效性。 作为首创的长效HIV衣壳抑制剂,Lenacapavir通过阻断病毒生命周期的关键环节来有效控制HIV-1的增殖。该药物在2022年8月首次在欧洲获得市场准入,并于同年12月获得美国FDA的批准,成为全球首个也是唯一一个每年仅需两次注射的HIV治疗药物。 吉利德所公布的数据来自其全面和多样化的PURPOSE临床项目,该项目共包括全球5项HIV预防试验,此次是PURPOSE项目产生的首批数据-PURPOSE 1。这是一项双盲、随机3期研究,目的是比较lenacapavir与Truvada和Descovy在16至25岁女性群体中作为PrEP(Pre-exposure Prophylaxis,暴露前预防)的安全性和效果。。 参与PURPOSE 1试验的受试者,包括来自南非25个地区和乌干达3个地区的5300余名16至25岁的年轻女性及青春期少女。参与者被随机分为三组,比例为2:2:1,分别接受了每年两次的Lenacapavir皮下注射,每日一次的Descovy口服治疗(恩曲他滨200mg/丙酚替诺福韦25mg),以及每日一次的Truvada口服治疗(恩曲他滨200mg/富马酸替诺福韦二吡呋酯300mg)。 临床试验结果显示,Lenacapavir组的2134名女性未发现HIV感染案例;相比之下,Truvada组的1068名女性中有16起感染事件(发病率为1.69每100人年),Descovy组的2136名女性中有39起感染事件(发病率为2.02每100人年)。Lenacapavir不仅优于主要比较对象HIV基准感染率bHIV(发病率为2.41每100人年)和Truvada(次要对照组),不仅成功实现了研究的主要和次要目标,还显示出优异的整体耐受性,并没有发现任何重大或新的安全问题。 当前,吉利德正在进行其他旨在评估lenacapavir作为PrEP用途的PURPOSE临床试验。公司计划在2024年年末或2025年年初发布另一项关键试验PURPOSE2的结果,该试验旨在评估半年一次的lenacapavir注射在预防HIV感染方面对不同性别取向的男女个体的有效性。若PURPOSE1和PURPOSE2的试验结果均呈正面,吉利德将把这两项试验的数据纳入lenacapavir作为HIV PrEP疗法的监管申请中,以确保该药物能获得批准,服务于那些迫切需要更多HIV预防选项的多样化群体。 虽然Lenacapavir本质上是一种长效药物,但其注射频率与某些疫苗相似,并且其100%的有效率远远超过了任何HIV试验性疫苗,因此市场上将其视为一种“疫苗”也就不足为奇了。 当然,将Lenacapavir称为“疫苗”只是一种比喻。然而,这种比喻背后所隐含的深层意义,实际上预示着HIV防治领域的一次重大转变。 毕竟,这是人类抗击艾滋病历史上首次公布的零感染率的HIV预防三期临床试验,Lenacapavir每年仅需两次注射,具有显著的依从性优势,标志着一项具有里程碑意义的新突破,有望成为一款颠覆性新药。 前衍可提供产品 2189684-44-2 HIV-1衣壳抑制剂Lenacapavir 143491-57-0 恩曲他滨 147127-20-6 替诺福韦
2024-07-17
2024上半年FDA批准的新化药
2024年上半年CDER批准了21个新分子实体,其中15种为化学合成药物,6种为生物制剂。 值得注意的是,与去年同期相比,今年上半年获批的新药数量显著减少,2023年同期已有26种新分子药物获得批准。 2024上半年,CDER批准的化药新药 在审批流程中,15种新化学药物中有8种药物是通过优先审评获批上市的,相较于常规审批流程需要10个月,优先审评要求在6个月内完成,这些药物通常因其较高的治疗价值而获得优先考虑。 从适应症角度分析,5种药物针对代谢性疾病,3种针对肿瘤,免疫治疗、抗感染以及其他类别各有2种,神经系统疾病有1种。在这些新化学药物中,孤儿药有6种,占比接近一半,这反映出罕见病治疗领域的研发热情依然高涨。 接下来,根据公开的资料,简要概述一些新近获批的新化学药品。 Iqirvo(Elafibranor) 6月10日,益普生公司宣布,美国食品药品监督管理局(FDA)已迅速批准了Iqirvo的上市申请。Iqirvo是一种首创的口服PPAR激动剂,每日服用一次,适用于治疗那些对UDCA反应不佳的成人原发性胆汁性胆管炎(PBC)患者,或者作为单一治疗方案,用于治疗那些对UDCA不耐受的患者。PBC是一种罕见的肝脏疾病,在美国大约影响10万人,有可能导致肝功能衰竭。 这是近十年来首个获得批准用于治疗罕见肝病原发性胆汁性胆管炎的新药。 Iqirvo的快速批准是基于《新英格兰医学杂志》上发表的III期ELATIVE临床试验结果。值得一提的是,同一靶点的药物Seladelpar,也已被FDA纳入优先审评程序,预计将在8月宣布其审评结果。 Ojemda(Tovorafenib) 4月23日,FDA快速批准了Day One Biopharmaceuticals研发的广谱RAF激酶抑制剂Ojemda(tovorafenib),用于治疗6个月以上患有复发性或难治性儿童低级别胶质瘤(pLGG)的患者,特别是那些携带BRAF基因融合、重排或V600突变的患者。儿科低级别胶质瘤是儿童中最常见的脑瘤,根据统计,美国儿童每年每十万人中有1.3至2.1例新发病例,预计每年新增1000至1600例。2023年3月16日,FDA已经批准了诺华公司的BRAF/MEK联合疗法,包括Tafinlar(dabrafenib,达拉非尼)和Mekinist(trametinib,曲美替尼)。 这是pLGG的首个靶向疗法。 Tovorafenib是一种口服的、能够穿透血脑屏障的、选择性广谱Raf抑制剂,用于针对 MAPK 信号通路中的关键酶,以治疗儿童复发性或难治性低级别胶质瘤。Ojemda作为一种全身性治疗手段,能有效阻止携带BRAF基因融合或V600突变的肿瘤细胞增殖,并且具备穿透大脑的能力。该药物之前因其在FIREFLY-1临床2期试验中的表现,被FDA认定为突破性疗法,并获得了罕见儿科疾病治疗资格。 Xolremdi(Mavorixafor) 4月26日,X4 Pharmaceuticals公司宣布,FDA已批准Xolremdi(mavorixafor)胶囊上市,用于治疗12岁及以上的WHIM综合征患者,目的是提升血液中成熟中性粒细胞和淋巴细胞的水平。WHIM综合征是一种罕见的原发性免疫缺陷病,伴随慢性中性粒细胞减少,其名称来源于其主要症状:疣,低丙种球蛋白血症,感染和骨髓细胞增多症。 这是首款获批针对WHIM综合征患者的小分子疗法。 Mavorixafor作为CXC趋化因子受体4(CXCR4)的口服可用拮抗剂,在III期4WHIM临床试验中显示出显著效果,与安慰剂组相比,使用Xolremdi的患者年感染率显著下降60%,年感染次数降至不足一次,而安慰剂组则高达4.5次。随着治疗的持续,感染率的降低效果更为显著。 Duvyzat(Givinostat) 3月21日,FDA批准Italfarmaco/ITF的口服药物Duvyzat(givinostat),该药用于治疗六岁及以上的杜氏肌营养不良症(DMD)患者。Givinostat作为组蛋白去乙酰化酶(HDAC)的抑制剂,其作用机制是通过靶向致病过程,以减轻炎症反应和肌肉组织的损伤。 这是第一个被批准用于治疗所有 DMD 基因变异患者的非甾体药物。 Duvyzat的批准基于一项III期临床研究的成功,该研究不仅实现了从基线到72周的四级爬升评估的主要目标,还在多个关键的次要评价标准上呈现出积极的结果。 Rezdiffra(Resmetirom) 3月14日,代谢功能障碍相关脂肪性肝炎(MASH)治疗领域取得了重大进展,FDA批准了Madrigal公司研发的Rezdiffra口服小分子药物,用于治疗存在中度至重度肝纤维化的成人患者,该药物需与健康饮食和规律运动相结合使用。 这是40年来首款获批上市的MASH药物。 Resmetirom作为甲状腺激素受体-β (THR-β) 的一种可口服选择性激活剂。在III期MAESTRO-NASH临床试验中展现了显著效果,25.9%接受80 mg剂量和29.9%接受100 mg剂量的患者在治疗后MASH症状得到缓解,且未观察到肝纤维化的进一步恶化。 今年上半年,抗肿瘤、自身免疫疾病、代谢疾病、抗感染和罕见病仍然是FDA批准新药的热点领域。未来的下半年突破还在继续,FDA又会批准哪些新药呢,让我们期待吧! 前衍可提供的实验用小分子化合物 1195765-45-7 达拉非尼 871700-17-3 曲美替尼 920509-32-6 Resmetirom 558447-26-0 Mavorixafor 851528-79-5 Seladelpar 923978-27-2 Elafibranor 伊拉贝诺
2024-07-10